


W O D Ó R
Jak się okazuje, składniki naszego "misia" są bardzo proste i mają jeszcze jedną cechę: otóż jeżeli mamy osobno tlen i osobno wodór, to możemy przeprowadzić reakcję spalania wodoru w tymże tlenie (reakcja syntezy), w wyniku czego uzyskujemy... wodę! Ale oczywiście, naszym celem nie jest uzyskiwanie tą drogą wody, której mamy pod dostatkiem z innych źródeł. Efektem ubocznym reakcji łączenia się tlenu z wodorem jest ogromna ilość energii, i ta właśnie energia interesuje nas najbardziej. Proszę się przyjrzeć tej reakcji:
2H2 + O2 ---> 2H2O 
Substratami są tlen (którego mamy pod dostatkiem w naszej atmosferze) oraz nietoksyczny, czysty wodór, który jako neutralny gaz nie zanieczyszcza wody, ziemi i powietrza. Produktem jest czysta woda, która w żaden sposób nie może być porównywana ze spalinami uzyskiwanymi przy spalaniu paliw węglowodorowych.
Jedyny problem to skąd wziąć wodór? Nie można go bowiem wydobyć, nie występuje również w większych ilościach w naturze. Oczywiście najlepszym źródłem wodoru jest sama woda, ale żeby rozłożyć wodę z powrotem do tlenu i wodoru potrzeba energii. Energię taką możemy uzyskać np. ze Słońca, wody lub powietrza budując odpowiednio elektrownie słoneczne, wodne czy wiatrowe.
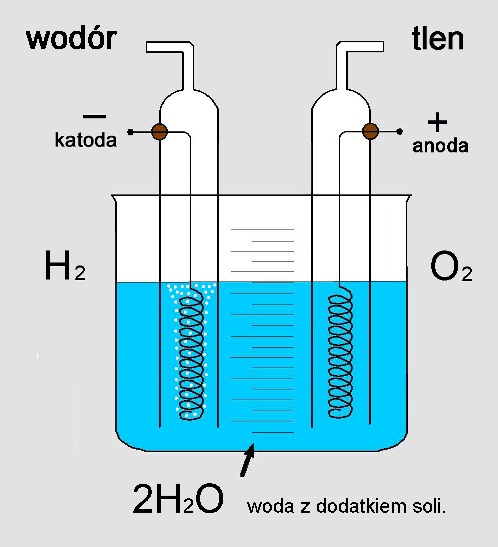
Aby rozbić cząsteczkę wody na wodór i tlen , wykorzystuje się zjawisko elektrolizy, a więc rozkładu cząsteczki pod wpływem elektronów pochodzących od przepływającego przez wodny roztwór soli prądu elektrycznego. Na jednej elektrodzie wytwarza się tlen, a na drugiej wodór. Rozdzielając przestrzeń między tymi dwoma elektrodami możemy uzyskiwać czysty tlen i wodór. Tlen możemy wykorzystać w dowolnej innej technologii, natomiast powstały gazowy wodór możemy sprężyć i przechowywać, a następnie wykorzystać do dowolnych celów.
Paliwo wodorowe ma prawie same zalety: od niskiej toksyczności po nieszkodliwe produkty spalania, jedyną wadą albo i zaletą jest postać gazowa oraz łatwość w zapaleniu się od małej iskry.
Jednym z najważniejszych aspektów przemawiających za stosowaniem wodoru jako paliwa w transporcie i energetyce jest ochrona środowiska, ponieważ wodór jest paliwem bez emisyjnym. Zastosowanie tego gazu w znaczący sposób ułatwi walkę z problem smogu w coraz większych metropoliach. Ważnym problemem globalnym jest też efekt cieplarniany, za co jest odpowiedzialna emisja CO2 do atmosfery, co niema miejsca w przypadku pojazdów napędzanych wodorem oraz elektrowni. Wobec powyższych faktów zastosowanie wodoru, jako nośnika energii w połączeniu z ekologicznymi formami jego wytwarzania, daje możliwość radykalnego zmniejszenia emisji CO2.
Podstawowe właściwości fizyczne wodoru
Atom wodoru, jako pierwiastek składa się z protonu i elektronu. W postaci gazowej tworzy dwuatomowe cząsteczki. Jest jednym z najbardziej powszechnych pierwiastków, około 75% masy materii we Wszechświecie to wodór.
Cechy fizyczne wodoru:
- Czysty wodór jest bezbarwny i bezwonny,
- Jest gazem nie toksycznym lecz bardzo łatwo łączy się z tlenem tworząc mieszankę wybuchową, a w zamkniętych pomieszczeniach może spowodować duszenie.
- Punkt wrzenia wodoru wynosi 20 `K (423 `F; 253 `C) przy ciśnieniu jednej atmosfery.
- Gęstość jest jedną z najważniejszych cech wodoru pod katem zastosowania jako paliwa. W postaci gazowej gęstość wodoru wynosi 0,08376 kg/m3 (293 0K, 1 atm). W postaci ciekłej gęstość wynosi 70,8 kg/m3 (20 `K, 1 atm).
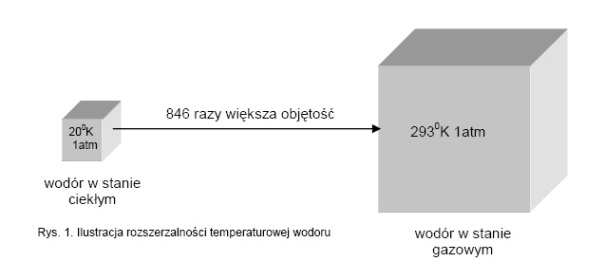
Duża rozszerzalność temperaturowa wodoru, ilustruje rysunek nr 1.
 |
Produkcja i wykorzystanie wodoru jako paliwa są od lat analizowane i planowane. Programy badań w tym zakresie są szeroko realizowane w USA, Japonii oraz w Unii Europejskiej.
Charakterystycznymi parametrami wodoru są:
1. wartość opałowa,
2. granice palności,
3. liczba oktanowa,
4. prędkość spalania,
5. temperatura samo-zapłonu,
6. odległość krytyczna propagacji płomienia,
7. energia zapłonu.
1. Wartość opałowa.
Wartość opałowa jest to ilość ciepła powstała podczas całkowitego i zupełnego spalenia jednostki paliwa ( m3 lub kg wodoru) przy założeniu, że spaliny zostały ochłodzone do temperatury pierwotnej substratów, a woda znajdująca się w spalinach jest w postaci pary.
Na podstawie tabeli nr 1 widzimy, że wartość opałowa wodoru jest dwukrotnie większa od wartości opałowej metanu, propanu, benzyny czy oleju napędowego. Pamiętać trzeba jednak, że gęstość wodoru w warunkach normalnych jest dużo mniejsza niż metanu i znacznie mniejsza od gęstości benzyny czy ropy.
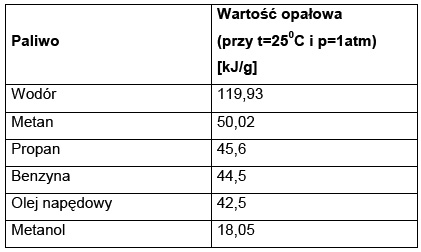 |
Tabela Nr 1 wartość opałowa dla różnych paliw.
2. Granice palności.
Ważnymi parametrami charakterystycznymi paliwa są granice palności. Pod tym pojęciem rozumiemy stosunek wodoru do powietrza przy którym następuje zapłon mieszanki. W przypadku wodoru obejmuje one zakres od 4% do 75% zawartości wodoru w powietrzu (Rys. 2.).
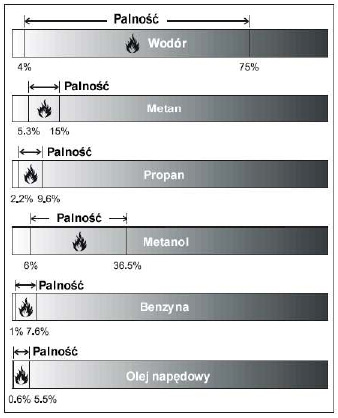 |
Rys. 2. Granice palności wodoru
Widzimy, że wodór może się palić w bardzo dużym zakresie koncentracji mieszanki wodór-powietrze. W porównaniu do innych paliw, takich jak benzyna czy olej napędowy zakres palności wodoru jest kilkakrotnie większy. Plusem jest to, że dolna granica palności dla wodoru wynosi 4%, a dla oparów oleju napędowego tylko 0,6% a benzyny 1%, co oznacza że wodór przy małych stężeniach jest bezpieczniejszy.
3. Liczba oktanowa
Liczba oktanowa określa jakość paliwa dla silników z zapłonem iskrowym lub turbinowym. Parametr ten określa odporność mieszanki paliwowo-powietrznej na samozapłon i spalanie detonacyjne podczas sprężania mieszanki oraz podczas rozpoczętego już procesu spalania mieszanki w cylindrze silnika. Jak widać z poniższego zestawienia (tabela nr 2) wartość liczby oktanowej dla wodoru jest bardzo wysoka . Z faktu tego należy wysnuć wniosek, że mieszanka wodorowo-powietrzna jest bardzo odporna na samozapłon i spalanie detonacyjne.
Dlatego też idealnie nadaje się do stosowania w silnikach spalinowych z zapłonem iskrowym, dyskwalifikuje ja jednak do silników Diesla w przeciwieństwie do oleju napędowego, który liczbę oktanowa ma bardzo małą.
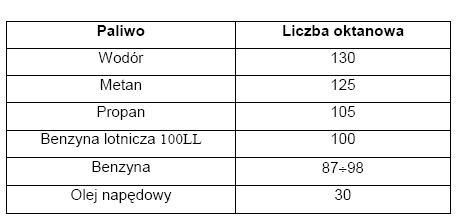 |
Tabela nr 2. Zestawienie liczb oktanowych równych paliw.
4. Prędkość spalania.
Prędkość spalania charakteryzuje nam dynamikę procesu spalania. Prędkość spalania dla mieszanki wodorowo-powietrznej wynosi 2,65 3,25 m/s. Dla mieszanek benzyny z powietrzem wynosi 0,37 0,43 m/s a metanu z powietrzem 0,37 0,45 m/s. Z powyższego zestawienia wynika wniosek, że dynamika procesu spalania wodoru jest dużo wyższa niż innych paliw.
5. Temperatura samozapłonu.
Temperatura samozapłonu jest to temperatura przy której ciepło wydzielone z reakcji utlenienia w jednostce czasu jest równe ciepłu wypromieniowanemu do otoczenia. Powyżej tej temperatury następuje gwałtowny wzrost prędkości reakcji utleniania i wydzielania się dużych ilości ciepła. Dla wodoru temperatura samozapłonu jest relatywnie wysoka w porównaniu z innymi paliwami, co ilustruje tabela nr 3.
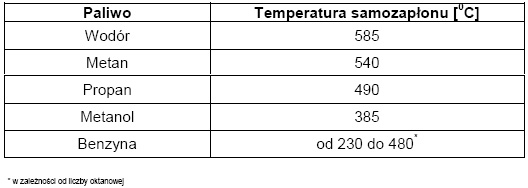 |
Tabela nr 3. Zestawienie temperatur samozapłonu
6. Odległość krytyczna propagacji płomienia (Quenchingdistance).
Odległość krytyczna to minimalna szerokość szczeliny przy której nie występuje dalsza propagacja otwartego płomienia w mieszance paliwowo powietrznej. W warunkach normalnych dla mieszanki wodoru z powietrzem dystans ten wynosi 0,6mm. Dla porównania - dla mieszanki propanu, butanu lub benzyny z powietrzem dystans ten wynosi 2mm. Efekt ten jest spowodowany przez ochładzanie płomienia przez ścianki szczeliny.
Tabela nr 4. Zestawienie odległości krytycznej dla różnych paliw.
 |
Odległość krytyczna zależy od mieszanki, temperatury, ciśnienia oraz od kształtu szczeliny paliw (tabela nr 4).
7. Energia zapłonu.
Energia zapłonu jest to najmniejsza wartość energii wyładowania iskrowego, jaka w danych warunkach może spowodować zapłon lub wybuch mieszaniny wybuchowej. Energia zapłonu wodoru wynosi tylko 0,02 mJ, o jeden rząd wielkości mniej niż gazu ziemnego (0,29 mJ) lub propanu (0,26mJ)
Z powyższego zestawienia wynika, że wodór idealnie nadaje się do silników iskrowych i turbinowych.
Analiza stechiometryczna procesu spalania.
Spalanie wodoru przebiega według poniższej reakcji.
2H2+O2 2H2O (1)
W celu obliczenia zapotrzebowania powietrza (rachunek objętościowy), należy najpierw obliczyć ilość tlenu potrzebnego do utlenienia wodoru. Obliczenie potrzebnego tlenu wykonujemy dla warunków normalnych ( p=0,1 Mpa , T=273,15K). Wodór zgodnie ze wzorem stechiometrycznym spala się w proporcji 1:2. W związku z tym względna objętość tlenu przypadająca na m3 wodoru (tzw. tlen teoretyczny)
będzie wynosić:
Ot=0,5*H2 [m3o2/m3 paliwa] (2)
W celu obliczenia względnej objętości potrzebnego powietrza (powietrza teoretycznego) należy uwzględnić zawartość azotu w powietrzu. Stosunek objętości powietrza do zawartego w nim tlenu wynosi 100/21, zatem objętość względna dla powietrza wynosi:
Vt=100/21*Ot =4,762*Ot [m3o2/m3 wodoru] (3)
a po uwzględnieniu (2) mamy:
Vt =4,762*0,5=2,42 [m3 powietrza/m3 wodoru] (4)
W związku z powyższym proporcja objętości względnej powietrza do objętości wodoru wynosi:
Vt /VH2=2,4 : 1 (5)
W celu obliczenia masy potrzebnego powietrza, należy w pierwszej kolejności obliczyć masę tlenu potrzebnego do utlenienia wodoru.
Masa jednego mola tlenu mO2= 1 mol x 32 g/mol =32g (6)
Masa jednego mola azotu
mN2=1 mol O2 x (79% N2 / 21% ) x 28 g/ mol (7)
= 3,762 mol x 28 g/mol = 105,33 g
Masa jednego mola powietrza mpowietrza = mN2+m02 = 32g + 105,33 g =137 g (8)
Masa jednego mola wodoru mH2=2 mol H2 x 2 g/mol = 4g (9)
Stad proporcja masy powietrza do masy wodoru wynosi
mpowietrza/m H2 = 137,33g / 4g = 34,33:1 (10)
Z powyższych obliczeń wynika, że do spalenia 1g wodoru musimy dostarczyć 34g powietrza. Dla spalenia 1g benzyny musimy dostarczyć tylko 14,7 g powietrza. Wynika stad, że układy zasysające powietrze w silnikach wodorowych musza być bardziej wydajne tlenowo niż w silnikach spalinowych.
Zbiorniki do przechowywania wodoru.
Zbiorniki na sprężony wodór to najbardziej powszechne i dopracowane technologicznie zbiorniki. Takie zbiorniki są obecnie powszechnie stosowane w motoryzacji. Sprężony wodór magazynowany jest w cylindrycznym zbiorniku bardzo podobnym do zbiorników używanych do paliw LPG.
Zbiornik wysokociśnieniowy. Najczęściej stosowana jest konstrukcja, w której wewnętrzna warstwa wykonana jest z aluminium lub stali (20% całkowitej masy) zalana od zewnątrz tworzywem kompozytowym. Taki rodzaj zbiornika cechuje się wysoka odpornością na uszkodzenia mechaniczne oraz stosunkowo małą masą w porównaniu do innych zbiorników.
Rysunek 3 przedstawia konstrukcje zbiornika, w którym wewnętrzny cylinder wykonany jest z aluminium. Wewnętrzny cylinder powleczony jest heliakalnie skręconymi włóknamiwęglowymi . Do spojenia włókien stosuje się żywice epoksydowa. Zewnętrzna warstwa dodatkowo jest pokryta włóknami w kształcie obręczy. Kompozyt nadaje zbiornikowi elastyczność, zwiększając przez to odporność na uszkodzenia mechaniczne. Wewnętrzna warstwa zrobiona jest z polimeru.
 |
Rys 3. Zbiornik wysokociśnieniowy.
Zbiornik firmy Quantum (rys.4.) wyposażony jest również w specjalna warstwę przeciwuderzeniową, warstwy zewnętrzne zrobione są z włókien węglowych zalanych żywicą epoksydową.
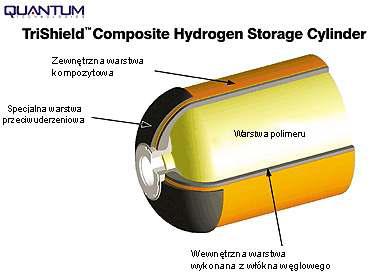 |
Rys. 4. Kompozytowy zbiornik firmy Quantum.
Zbiorniki tego typu wykonane są w kilku wersjach: dla ciśnień 250 bar 350 bar, oraz 700 bar. Warto zwrócić uwagę, że ok. 5% (~7000 kJ/kg) energii zawartej w wodorze musi zostać poświecona na jego kompresje do ciśnienia 350 bar. Dlatego istotny jest sposób konstrukcji.
Budowa stacji wodorowej.
Na zdjęciu poniżej przedstawiona jest stacja wodorowa znajdująca się na lotnisku Monachium.
Powyższa stacja wodorowa została zaprojektowana pod kątem tankowania samochodów na ciekły lub gazowy wodór. Wodór w postaci gazowej tankowany jest do autobusu firmy MAN wyposażonego w zbiornik wysoko ciśnieniowy CGH2 oraz silnik spalinowy z zapłonem iskrowym. Ciekły wodór tankowany jest do samochodu osobowego firmy BMW również wyposażonego w silnik spalinowy. Dlatego też na stacji istnieją dwa oddzielne systemy magazynowania wodoru. Jeden z nich służy do przechowywania gazowego wodoru o pojemności 2000 m3 gazu i zbiorników wysokociśnieniowych (35 MPa) o łącznej pojemności 10 m3 gazu. Drugi to termoizolacyjny zbiornik na ciekły wodór o pojemności 12000 litrów. Stacja wyposażona jest w elektrolizer wytwarzający gazowy wodór. Ciekły wodór produkowany jest też w pobliskiej wytwórni wodoru firmy Linde i transportowany rurociągiem (~ 3 km) do stacji.
 |
Stacja wodorowa na lotnisku w Monachium.
W większości stacji, wodór gazowy wytwarzany jest na miejscu przy pomocy elektrolizera. W przypadku dystrybucji ciekłego wodoru LH2, wodór dowożony jest do stacji przy pomocy cystern lub dostarczany rurociągiem.
 |
Autobus MAN tankuje wodór na stacji wodorowej.
Proszę zauważyć, że zbiornik z wodorem umieszczony jest na dachu w środkowej części pojazdu, co powoduje iż pojazd podczas kolizji jest całkowicie bezpieczny, a paliwo wodorowe poprzez zawór bezpieczeństwa może ulec opróżnieniu. Opróżnienie zbiornika z wodorem zajmuje około 1 sekundy.
